Neues Werkzeugset revolutioniert Erforschung von IRES-Elementen für mRNA-Therapien
Ella Becker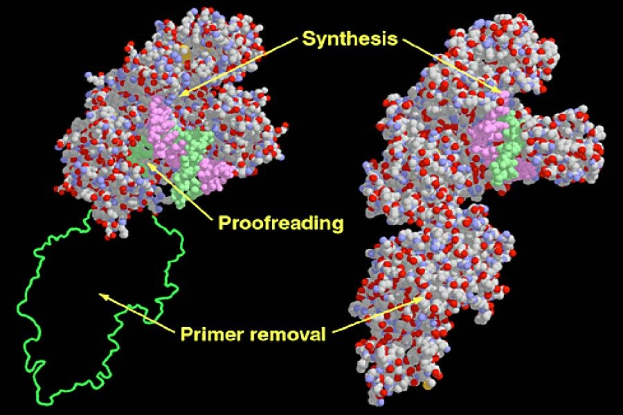
Neues Werkzeugset revolutioniert Erforschung von IRES-Elementen für mRNA-Therapien
Forscher des Universitätsklinikums Bonn, der Universität Bonn und der Stanford University haben ein neues Werkzeugset zur Erforschung interner ribosomaler Eintrittsstellen (IRES) entwickelt. Der Durchbruch soll einen Goldstandard für die Identifizierung starker IRES-Elemente setzen, die für die synthetische Biologie und die Entwicklung mRNA-basierter Therapien von zentraler Bedeutung sind.
IRES-Elemente spielen eine Schlüsselrolle bei der Initiation der Translation und ermöglichen die Proteinproduktion selbst dann, wenn die übliche 5'-Cap-Struktur der mRNA blockiert ist – etwa während viraler Infektionen. Zudem tragen sie zur Regulation der Genexpression bei, wobei das Ribosom als aktiver Kontrolleur der Proteinsynthese fungiert.
Die von Prof. Kathrin Leppek geleitete Forschungsgruppe „Immunbiochemie“ untersucht, wie Ribosomen direkt mit mRNAs interagieren, um die Translation zu steuern. Bisher fehlte in diesem Bereich jedoch eine zuverlässige, einheitliche Methode zur Charakterisierung „zellulärer IRES-Elemente“.
Das neu entwickelte Werkzeugset führt fortschrittliche Techniken ein, darunter zirkuläre RNA-Reporter und die quantitative Färbung einzelner mRNA-Moleküle. Dieser Ansatz verbessert die Genauigkeit bei der Erkennung von IRES-Elementen. Die beteiligten Einrichtungen – Universitätsklinikum Bonn, Universität Bonn und Stanford – haben zudem wirksame nicht-virale IRES-Sequenzen patentiert, die die Translation in zirkulären RNAs verstärken.
Die Finanzierung des Projekts erfolgte durch die Deutsche Forschungsgemeinschaft (DFG) und die Universität Bonn.
Das Werkzeugset bietet eine standardisierte Methode zur Identifizierung und Bewertung von IRES-Elementen und schließt damit eine lang bestehende Lücke in der Forschung. Die neuen Verfahren könnten den Fortschritt in der synthetischen Biologie und bei der Entwicklung mRNA-basierter Therapien beschleunigen. Die patentierten Sequenzen könnten zudem die Effizienz von Anwendungen mit zirkulärer RNA steigern.